Ácido-base

Características generales
La muestra requerida es de sangre arterial o venosa en jeringa con heparina de litio balanceada. La medición se realiza en plasma (no en suero) con anticoagulante no ácido-base (heparina), dado que la cascada de la coagulación produce reacciones ácido-base que pudieran afectar la interpretación.
El pH arterial es similar al periférico, pero no la PCO2 ni tampoco el HCO3 cuando se obtiene desde un cálculo. Dado que la sangre venosa tiene mayor contenido de CO2, esto aumenta el HCO3 y disminuye el pH. Para una correcta interpretación ácido-base se requieren gases arteriales.
Muestra | pH | [H+] (nEq/L) | PCO2 (mmHg) | HCO3- (mEq/L) |
Arterial | 7,4 (7,36-7,44) | 40 (36-44) | 40 (36-44) | 24 (22-26) |
Venosa | 7,38 (7,34-7,42) | 42 (38-46) | 46 (42-50) | 26 (24-28) |
Se deben mantener las condiciones anaeróbicas de la muestra, eliminando todas las burbujas de la jeringa, dado que el contacto con aire produce pérdida de CO2.
Idealmente el paciente debe estar en un estado de “equilibrio ventilatorio”, por lo que si han habido cambios por ejercicio o de FiO2 se debe esperar al menos 20 minutos. El CO2 venoso aumenta considerablemente cuando proviene de una extremidad mal perfundida, por lo que se recomienda evitar compresión prolongada de extremidad al obtener la muestra.
El metabolismo celular altera el estado ácido-base de la muestra, por lo que se debe favorecer el transporte y lectura inmediata (<15-30 min) de la misma. Los errores en la manipulación de la muestra simulan trastornos respiratorios agudos.
Enfoque estructurado para el diagnóstico de pacientes con trastornos acido-básicos
1. Evaluación clínica inicial
Conocer el cuadro clínico del paciente (es decir, la historia, examen físico y exámenes iniciales) permite orientar hacia el o los trastornos ácido-base más probables. El conocimiento de la fisiopatología de las posibles condiciones subyacentes resulta útil para su interpretación. Es importante considerar que en algunos escenarios la historia puede ser inadecuada o engañosa y que el rango de diagnósticos posibles puede ser muy amplio. Por otra parte, el enfrentamiento de los trastornos mixtos suele ser difícil: la historia y el examen por sí solos suelen ser insuficientes para clasificarlos.
2. Interpretación del estado ácido-base
Realizar una evaluación sistemática de los gases en sangre (con pH, PaCO2, PaO2 y Bicarbonato real) y otros resultados (Electrolitos plasmáticos y Albúmina plasmática) permite elaborar un diagnóstico ácido-base.
3. Diagnóstico clínico
Sintetizar la información recabada en los pasos previos para hacer un diagnóstico clínico global.
Elementos necesarios para correcta interpretación
- Conocer el cuadro clínico del paciente
- Examen de gases arteriales con:
- pH
- PaCO2
- PaO2
- Bicarbonato real
- Electrolitos plasmáticos
- Albúmina plasmática
Definiciones
La acidemia y la alcalemia se refieren a estados fisiológicos meramente dependientes del pH arterial. Existe acidemia si el pH es <7,35 y alcalemia si el pH es >7,45. Un paciente puede estar acidémico o alcalémico, no ambos.
La acidosis y la alcalosis hacen referencia a procesos que llevan al pH hacia la acidemia y alcalemia, respectivamente. Un paciente puede tener de forma concomitante estos trastornos.
Pasos para la interpretación del estado ácido base
1. Evaluar pH
- Si el pH es <7,35 hay una acidemia (y al menos una acidosis en curso)
- Si el pH es >7,45 hay una alcalemia (y al menos una alcalosis en curso)
- Si el pH es normal existen dos posibilidades:
- ausencia de trastorno ácido-base
- trastorno mixto (acidosis y alcalosis concomitantes)
- Siempre que se encuentre una alteración en la PaCO2 y/o HCO3– existirá un trastorno ácido-base.
2. Evaluar PaCO2
- Si la PaCO2 está alterada en la misma dirección que el pH, existe un trastorno ácido-base metabólico (pero no se puede excluir un trastorno mixto)
- Si la PaCO2 está alterada en dirección opuesta al pH, existe un trastorno ácido-base respiratorio (pero no se puede excluir un trastorno mixto)
3. Evaluar compensación y presencia de trastornos mixtos
Existen distintas formas de evaluar la compensación de un trastorno ácido-base:
| Trastorno | Compensación | Tiempo de instalación de compensación | Límite de compensación | |||
| Acidosis metabólica | PaCO2 = 2 últimos dígitos del pH ↓ PaCO2 en 1.25 (=5/4) mmHg por cada 1 mEq/L ↓ en [HCO3-] ↓ PaCO2 en 1,2 mmHg por cada 1 mEq/L ↓ en [HCO3-] PaCO2 = (1,5 · [HCO3-] + 8) | pH ↓ | PaCO2 ↓ | HCO3- ↓ | 24 h | PaCO2= 15 mmHg |
| Alcalosis metabólica | ↑ PaCO2 en 0,75 (=3/4) mmHg por cada 1 mEq/L ↑ en [HCO3-] ↑ PaCO2 en 0,6 mmHg por cada 1 mEq/L ↑ en [HCO3-] PaCO2 = (0,7 · [HCO3-] + 20) | pH ↑ | PaCO2 ↑ | HCO3- ↑ | 24 h | PaCO2 = 55 mmHg |
| Acidosis respiratoria aguda | ↑ [HCO3-] en 0,1 mEq/L por cada 1 mmHg ↑ en PaCO2 | pH ↓ | PaCO2 ↑ | HCO3- ↑ | 10 min | [HCO3-] = 38 mEq/L |
| Acidosis respiratoria crónica | ↑ [HCO3-] en 0,4 mEq/L por cada 1 mmHg ↑ en PaCO2 | pH ↓ | PaCO2 ↑ | HCO3- ↑ | 3-5 d | [HCO3-] = 45 mEq/L |
| Alcalosis respiratoria aguda | ↓ [HCO3-] en 0,2 mEq/L por cada 1 mmHg ↓ en PaCO2 | pH ↑ | PaCO2 ↓ | HCO3- ↓ | 10 min | [HCO3-] = 18 mEq/L |
| Alcalosis respiratoria crónica | ↓ [HCO3-] en 0,5 mEq/L por cada 1 mmHg ↓ en PaCO2 | pH ↑ | PaCO2 ↓ | HCO3- ↓ | 2-3 d | [HCO3-] = 15 mEq/L |
Si la compensación no es adecuada o la PaCO2 y el bicarbonato real se mueven en direcciones opuestas, es importante sospechar un trastorno mixto. Es relevante conocer que la compensación tiene un límite y por tanto todo trastorno muy extremo tiende a presentarse de forma mixta por la imposibilidad de compensar la alteración primaria. Una evaluación basada en la historia, el examen físico y otros resultados permitirá orientar la identificación de qué cambios son primarios y cuáles compensatorios.
4. Evaluar otros resultados claves
Resulta necesario revisar otros resultados en busca de evidencia específica de trastornos particulares. En la mayoría de las circunstancias, estas claves confirman el diagnóstico esperado, pero en ocasiones pueden alertar sobre la presencia de un segundo trastorno no anticipado. La mayoría de estas claves se obtienen del perfil bioquímico.
Evaluación de anión gap (AG)
El anión gap (AG) es una herramienta para evaluación de trastornos ácido-base metabólicos que se sustenta en el principio de electroneutralidad, ya que la suma total de cationes debe ser la misma que aniones. Su valor normal es aproximadamente 10 ± 2. Un anión gap elevado usualmente traduce la producción de un ácido patológico, incluso en situaciones con pH normal (donde probablemente nos encontremos en presencia de un trastorno mixto).
[Na+] + [K+] + [Ca2+] + [Cationes no medidos] = [Cl–] + [HCO3–] + [Aniones no medidos]
Despejando la ecuación con los iones más prevalentes del plasma…
[Na+] – [Cl–] – [HCO3–] = [Aniones no medidos] – [Cationes no medidos]
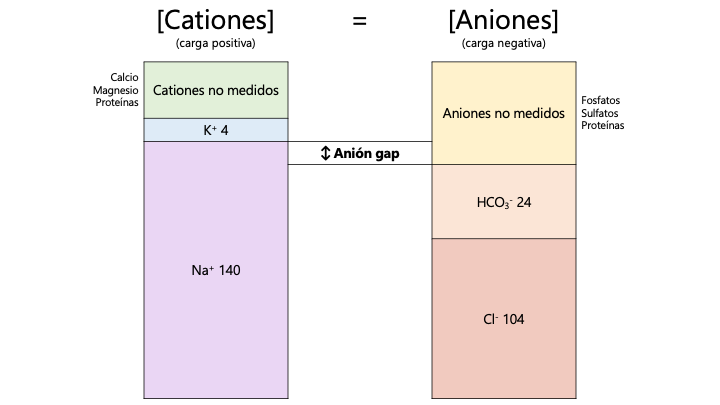
Como el Na+ es el principal catión del extracelular, el valor de los cationes no medidos es cercano a 0, sin embargo la cantidad de aniones no medidos es algo mayor, fundamentalmente por la albúmina.
Si se agrega un ácido, la base conjugada (anión orgánico) entrará a participar de los aniones no medidos, por lo tanto, el valor del AG aumentará. Esto no sucede para las acidosis hiperclorémicas (HCl), ya que su base conjugada (Cl–) sí es medida.
Es importante resaltar que gran parte del valor normal del AG se debe al “anión no medido” albúmina, si su concentración disminuye también lo hará el rango normal, motivo por el cual se corrige:
Anión gap (AG) | Na+ − Cl- − HCO3- |
Anión gap (AG) corregido | AG medido + 2,5 · (4,4 − Albúmina) |
Acidosis metabólica con AG aumentado | Acidosis metabólica con AG normal (hiperclorémica) |
|
|
Estudio de acidosis metabólica con anión gap elevado
En aquellas acidosis con AG aumentado, se buscarán las causas más frecuentes. Se evaluará el lactato arterial y cetonemia (betahidroxibutirato). Si la cetonemia y/o cetonuria son positivas, la etiología es una cetoacidosis diabética o ayuno. La hiperlactacidemia evidencia un estado de hipoperfusión severo. La elevación de ambos parámetros puede indicar una intoxicación por salicilatos o paracetamol, o una cetoacidosis con hiperlactacidemia. Si la cetonemia y lactacidemia son negativas, se evaluarán los parámetros de función renal, ya que la causa puede ser una insuficiencia renal aguda o crónica tardía.
Evaluación de ΔΔ gap y ΔΔ ratio
Una acidosis con AG aumentado se caracteriza por agregar aniones no medidos al medio, dado que los H+ provenientes del ácido reaccionan con HCO3–, disminuyendo su concentración. Por lo tanto, la cantidad de aniones no medidos adicionados deberá ser igual a la cantidad de HCO3– que disminuye. Una acidosis con AG normal no tendrá variaciones en los aniones no medidos.
El ΔΔ gap y el ΔΔ ratio permiten evaluar la presencia de trastornos con AG aumentado puros o mixtos, con valores intermedios reflejan procesos asociados que modifican las concentraciones de HCO3– o los aniones no medidos.
ΔΔ gap | ΔΔ gap = (AG − 10) − (24 − HCO3-) < -5: Trastorno puro o mixto:
-5 a 5: Acidosis metabólica con AG aumentado pura > 5: Trastorno puro o mixto:
|
ΔΔ ratio | ΔΔ = (AG − 10) / (24 − HCO3-) < 0,4: Acidosis metabólica hiperclorémica pura 0,4-1: Trastorno mixto:
1-2: Acidosis metabólica con AG aumentado pura >2: Trastorno mixto:
+
|
Evaluación de gap osmolar
En caso de acidosis metabólica con AG elevado en la que se ha descartado cetoacidosis, hiperlactatemia y falla renal, se debe buscar dirigidamente la ingesta de sustancias productoras de acidosis metabólica con AG aumentado. Los alcoholes son sustancias osmóticamente activas y las acidosis metabólicas con AG aumentado asociadas a éstos (metanol, etilenglicol, propilenglicol) se producen por la metabolización del osmol a un ácido.
Además del gap osmolar, se evaluarán las pruebas toxicológicas y la alcoholemia.
Gap osmolar | Osmolaridad medida - Osmolaridad calculada Osmolaridad medida - (2·Na+ + Glicemia/18 + BUN/2,8 + Alcoholemia/4,6) >10: sugiere la ingestión de sustancias (implica que existe un osmol generando la acidosis) >20: muy indicativo de ingesta de alcoholes (osmoles que después en el hígado se transforman en ácidos) <10: considerar intoxicación por salicilatos o paracetamol |
Estudio de acidosis metabólica con anión gap elevado
Evaluación de anión gap (AG) urinario
La acidosis metabólica hiperclorémica o con AG normal, debe ser analizada según el AG urinario.
La orina también obedece el principio de electroneutralidad. Los principales iones eliminados por la orina son K+, Na+ y Cl–. Cuando existe una acidosis, el riñón aumentará la excreción neta diaria de ácido de forma compensatoria, aumentando la síntesis y excreción de NH4+ principalmente (un catión no medido), cuyo anión acompañante será Cl–. La utilidad del AG urinario es permitir estimar indirectamente la cantidad de NH4+ excretado.
Los valores de aniones no medidos y cationes no medidos en orina de 24 horas son similares, por lo que el AG urinario normalmente es 0 mEq/día (una muestra de orina aislada tiene menor sensibilidad y el valor normal es 30 – 50 mEq/L).
| Anión gap urinario | [Na+]u + [K+]u + [Cationes no medidos]u = [Aniones no medidos]u + [Cl–]u [Na+]u + [K+]u – [Cl–]u = [Aniones no medidos]u – [Cationes no medidos]u |
Si el AG urinario tiene valor positivo (>0 mEq/día o >-20 mEq/L en orina aislada) indicará un defecto en la función renal, como insuficiencia renal temprana, ATR tipo I o ATR tipo IV (hipoaldosteronismo). Estas dos últimas se diferencian por el K+ plasmático, ya que en el hipoaldosteronismo existe hiperkalemia.
Cuando el AG urinario tiene valor negativo (<0 mEq/día o <-30 mEq/L en orina aislada), la acidificación distal se encuentra indemne, con excreción de amonio conservada. Por lo tanto, la acidosis puede ser secundaria a pérdidas digestivas de HCO3– o ATR tipo II. Esta última se caracteriza porque la excreción fraccionaria de HCO3– es >15%, a diferencia de las pérdidas digestivas de HCO3– donde este valor será prácticamente 0%.
El AG urinario no es útil en acidosis metabólica con AG aumentado, ya que la base conjugada se excreta por la orina (aniones no medidos) y altera los valores. Tampoco sirve si el VEC es bajo (se alteran los valores por menor aporte de Cl–). Si el pH urinario es muy alto (>6,5) pierde sensibilidad por la bicarbonaturia. La poliuria y la infección por bacterias que desdoblan urea a amonio también alteran los rangos.
5. Formulación de diagnóstico ácido-base completo
6. Realización de exámenes complementarios y/o confirmatorios
A veces, el diagnóstico requiere de pruebas adicionales para confirmar el diagnóstico o aumentar la precisión de la hipótesis diagnóstica. Los cambios en estos resultados pueden ser útiles para evaluar la magnitud del trastorno o la respuesta a la terapia. Ejemplos: lactato, cetonas urinarias, nivel de salicilatos, nivel de aldosterona, varios tests para evaluación de acidosis tubular renal.
Otras estrategias para enfocar el diagnóstico de pacientes con trastornos del equilibrio ácido-base
1. Realización de exámenes complementarios y/o confirmatorios
El delta de base buffer fue originalmente introducido por Singer y Hastings en 1948. Posteriormente, el exceso de base (EB) es un concepto propuesto por Siggaard-Andersen en 1960 como marcador independiente y fiable de acidosis/alcalosis metabólica, independiente de los trastornos respiratorios coexistentes y capaz de cuantificar la gravedad del trastorno. El EB se sustenta en el principio de electroneutralidad y la naturaleza bidireccional de las reacciones ácido-base y corresponde al “exceso” (ya sea positivo o negativo) de la base amortiguadora (suma de todos los aniones amortiguadores) real en comparación con la base amortiguadora normal, que se obtiene experimentalmente a través de procedimientos de equilibrio y titulación destinados a lograr condiciones normales de pH de 7,40 y PaCO2 de 40 mmHg. El EB es la cantidad de ácido/base (mmol/L) que debe agregarse a la muestra de sangre para alcanzar un pH de 7,40 en condiciones estandarizadas (PaCO2 40 mmHg, 37 °C). En general, el rango de BE entre −2 y +2 mmol/L se considera normal.
El EB es un parámetro útil para ayudar en el diagnóstico de trastornos metabólicos ácido-base y para evaluar cuantitativamente el desplazamiento metabólico. Si bien el EB corresponde a una valiosa estimación cuantitativa de los trastornos metabólicos ácido-base, no proporciona información alguna sobre los mecanismos patológicos subyacentes.
El EB estándar es otra técnica que permite hacer diagnóstico ácido-base y reemplaza al HCO3–, permitiendo evaluar el componente metabólico. Previamente se estimaba mediante un método físico-químico, en retirada dada la existencia de múltiples limitaciones para su uso. Actualmente, se calcula a partir del pH, PaCO2 y múltiples constantes que asumen “normalidad” en la Hb, estado del VEC, albúmina, fosfemia. Resulta relevante conocer que varios componentes contribuyen a su valor final (por ejemplo, cloruro, lactato, albúmina, cetoácidos), que eventualmente pueden operar en direcciones opuestas, anulándose entre sí y haciendo que la interpretación del valor de EB aislado sea difícil, dado que puede ser perfectamente normal en el caso de múltiples condiciones que actúen en direcciones opuestas. Mientras que un EB anormal es un marcador confiable de un problema metabólico activo, un EB normal no es suficiente para excluirlo.
El EB no puede considerarse un parámetro independiente y resulta fundamental complementarlo con mayor información para identificar trastornos ácido-base complejos. Pese a sus limitaciones es muy buen método, ampliamente utilizado en Europa.
2. Método físico-químico de Stewart
Esta evaluación se basa en la PaCO2 como componente respiratorio, la diferencia de iones fuertes (SID) como componente metabólico y la cuantificación total de bases débiles y sus aniones (A[tot]) como componente metabólico. Se utiliza principalmente en paciente crítico.
Revisores
Rodrigo Sepúlveda Palamara, Médico Internista y Nefrólogo Red Salud UC-Christus.
Joaquín Sharp Segovia, Médico Internista Red Salud UC-Christus.
Referencias
Strong E. ABG Interpretation: A Grand Overview of Acid-Base Analysis.
Sepúlveda R. Interpretación Ácido-Base.
Sistema de Información de Exámenes, SINFEX. Gases en Sangre Arterial.
Langer T, Brusatori S, Gattinoni L. Understanding base excess (BE): merits and pitfalls. Intensive Care Med. 2022 Aug;48(8):1080-1083.
Brandis K. Acid-base physiology [Internet]. Disponible en http://www.anaesthesiamcq.com/AcidBaseBook/ABindex.php
Bidani A, Tauzon DM, Heming TA: Regulation of whole body acid-base balance. In DuBose TD, Hamm LL, editors: Acid-base and electrolyte disorders: a companion to Brenner and Rector’s the kidney, Philadelphia, 2002, Saunders, pp 1-2.